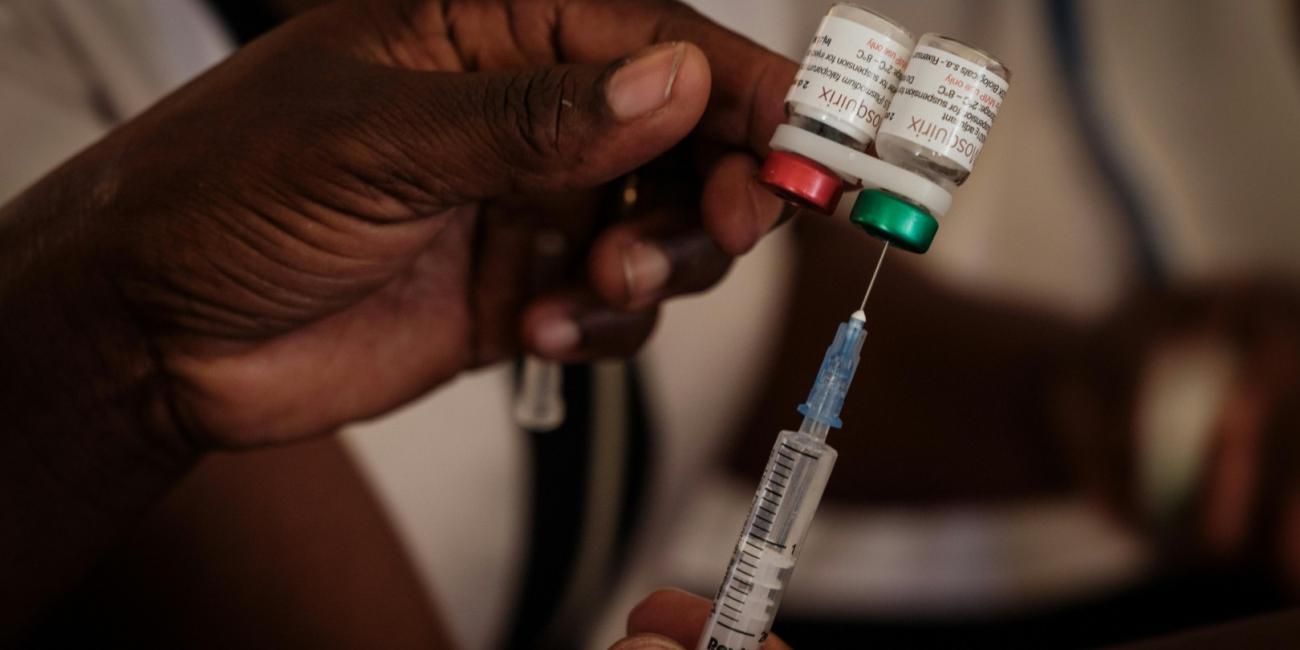
La FDA aprobó la talidomida recién en 1998 y advirtió contra su uso en mujeres embarazadas
- Este artículo data de hace más de cuatro años.
- Publicado el 15 de septiembre de 2021 a las 18:46
- Modificado el 15 de septiembre de 2021 a las 19:06
- 4 minutos de lectura
- Por AFP México
“Otro medicamento ‘experi-mentales’ fue el fármaco Talidomina. (...) La FDA también aprobó su uso, igual que las populares [vac]unas de hoy en día”, dice una de las publicaciones en Facebook (1, 2, 3) y Twitter (1, 2), junto a fotografías de niños con malformaciones en sus brazos.
Las entradas comenzaron a difundirse una semana después de que la FDA otorgó la aprobación total a la vacuna de Pfizer/BioNTech contra el covid-19 para mayores de 16 años.

La talidomida es un medicamento que se utiliza actualmente para tratar el mieloma múltiple, un cáncer de células plasmáticas, y también para aliviar y evitar síntomas cutáneos de la lepra, como llagas en la piel. El fármaco está contraindicado en mujeres embarazadas.
Fue sintetizado en 1953 por Wilhem Kunz en los laboratorios alemanes Chemie Grünenthal. Por sus propiedades hipnóticas y sedantes, se utilizó en países como Alemania, Canadá e Inglaterra para tratar las náuseas y los vómitos durante el embarazo como una alternativa a los barbitúricos, que generan adicción. En Estados Unidos, la talidomida fue administrada a varios cientos de mujeres embarazadas durante pruebas clínicas.
Una búsqueda en Google con las palabras clave “Aprobación Talidomida FDA” en inglés llevó a una entrada en la página web de la agencia estadounidense con información sobre el medicamento y el historial de su aprobación en Estados Unidos.
El enlace titulado “Historia regulatoria y etiquetado” condujo a un buscador de fármacos avalados. Al ingresar la palabra “Talidomida” en inglés, se obtuvieron solo dos registros de aprobación de este medicamento, el más antiguo de 1998, para la compañía Celgene.
En la sección “Historia y fechas de aprobación…”, se localizó el resumen de los dos procesos administrativos (1, 2) y en las respectivas cartas de aprobación se halló que el 16 de julio de 1998 la talidomida fue admitida por la FDA para tratar el eritema nudoso leproso y, el 25 de mayo de 2006, para tratar el mieloma múltiple.
En la etiqueta de la FDA para este medicamento fechada el 15 de julio de 1998 se lee: “Si la talidomida es tomada durante el embarazo, puede causar severos daños congénitos o la muerte de un bebé no nacido. (...) Nunca debe ser usada por mujeres embarazadas o que pudieran quedar embarazadas mientras tomen el fármaco”.
Rechazada en la década de 1960
Un rastreo en Google con la palabra “talidomida” en inglés limitado a resultados dentro del sitio de la FDA llevó a una nota titulada: “Frances Oldham Kelsey: revisora médica famosa por evitar una tragedia de salud pública”.
El texto cuenta que Kelsey, una especialista en farmacología que en 1960 comenzó a trabajar en la FDA, tuvo a su cargo entre sus primeras tareas analizar la solicitud de aprobación de la talidomida, la cual rechazó debido a la falta de evidencia presentada por la empresa William S. Merrel.
“La compañía continuó enviando lo que ellos consideraban que era una prueba de la seguridad de la talidomida, pero la Dra. Kelsey rotundamente insistió en evidencia científicamente confiable, de la cual ella sentía que la solicitud carecía profundamente. (...) Aproximadamente un año después, investigadores en Alemania y Australia relacionaron la talidomida con grupos de defectos congénitos graves y raros”, afirma la nota.
El artículo añade que Kelsey fue reconocida por el presidente John F. Kennedy en 1962 con el Premio Presidencial para el Servicio Civil Federal Distinguido. En el portal de la Biblioteca Presidencial y Museo John F. Kennedy, se localizó una fotografía de la entrega del premio y la transcripción de las palabras pronunciadas durante la ceremonia.
“Su excepcional juicio al evaluar la seguridad para uso en humanos de un nuevo medicamento ha prevenido una gran tragedia de deformidades congénitas en Estados Unidos”, dijo John W. Macy, secretario ejecutivo de la Junta encargada del reconocimiento, sobre Kelsey, según se lee en la tercera página de la transcripción.
Esta biografía de Kelsey menciona que la doctora Helen Taussig investigó en Europa los casos de malformaciones congénitas asociados al consumo de talidomida y luego testificó ante el Senado de Estados Unidos, lo que sirvió de apoyo a su postura.
Una búsqueda en Google con las palabras clave “Helen Taussig audiencia Senado” en inglés llevó a un documento con la transcripción de varias comparecencias ante la cámara alta, entre ellas una del 1 de agosto de 1962 sobre la coordinación entre agencias regulatorias de medicamentos.
En ella, el entonces comisionado de la FDA, George Larrick, hizo un recuento de las acciones tomadas por la agencia a su cargo en relación con la talidomida y declaró: “La talidomida no fue liberada por la FDA para su distribución comercial en Estados Unidos”.
En este documento también se encuentra una cronología de la solicitud de aprobación comercial de la talidomida en Estados Unidos hecha por la empresa William S. Merrell. Según esta, en septiembre de 1960 la farmacéutica envió información sobre ensayos clínicos con el medicamento a la FDA, pero la agencia pidió más información entre noviembre de 1960 y noviembre de 1961.
El 29 de noviembre de 1961 la empresa supo por primera vez de la posible asociación entre malformaciones congénitas y el consumo de talidomida, por lo que informaron a la FDA y finalizaron los ensayos clínicos.
Los efectos adversos causados por la talidomida motivaron la creación de las enmiendas Kefauver-Harris de 1962, reformas que fortalecieron el marco legal en relación con la seguridad y la efectividad de los medicamentos, señala la FDA.
Anteriormente, AFP Factual verificó publicaciones en redes sociales que erróneamente comparaban el desarrollo de las vacunas contra el covid-19 con la aprobación y el uso de la talidomida.
15 de septiembre de 2021 Agrega metadatos.
Copyright © AFP 2017-2025. Cualquier uso comercial de este contenido requiere una suscripción. Haga clic aquí para obtener más información.
¿Duda sobre la veracidad de una información, una foto o un video?
Contáctenos