Desinformación en torno al medicamento remdesivir y su aprobación puntual por la FDA
- Este artículo data de hace más de seis años.
- Publicado el 22 de mayo de 2020 a las 21:43
- Modificado el 22 de mayo de 2020 a las 22:02
- 5 minutos de lectura
- Por AFP Filipinas
- Traducción y adaptación: AFP México
El remdesivir “recién recibió la aprobación de la FDA, por lo que hasta este mes, comenzara a ser distribuido y utilizado de forma masiva, por lo que se espera poder frenar la ola de muertes (sic)”, dice una publicación del 2 de mayo de 2020, compartida más de 1.300 veces por usuarios de Facebook, según la herramienta CrowdTangle.
En la publicación del sitio web se afirma que “México fue pionero y ya realizo el primer pedido (sic)” y “el Gobierno de Victor Manuel Obrador (sic), no esperará o cuestionará la oportunidad y decidiera ordenar un gran contingente de este fármaco, para comenzar a atacar al Coronavirus”.
En otras publicaciones hay confusión respecto al uso del fármaco en el tratamiento del COVID-19. Algunos usuarios dicen en Twitter que se trata del diseño de una vacuna (1, 2, 3) y que México será parte de los ensayos clínicos.
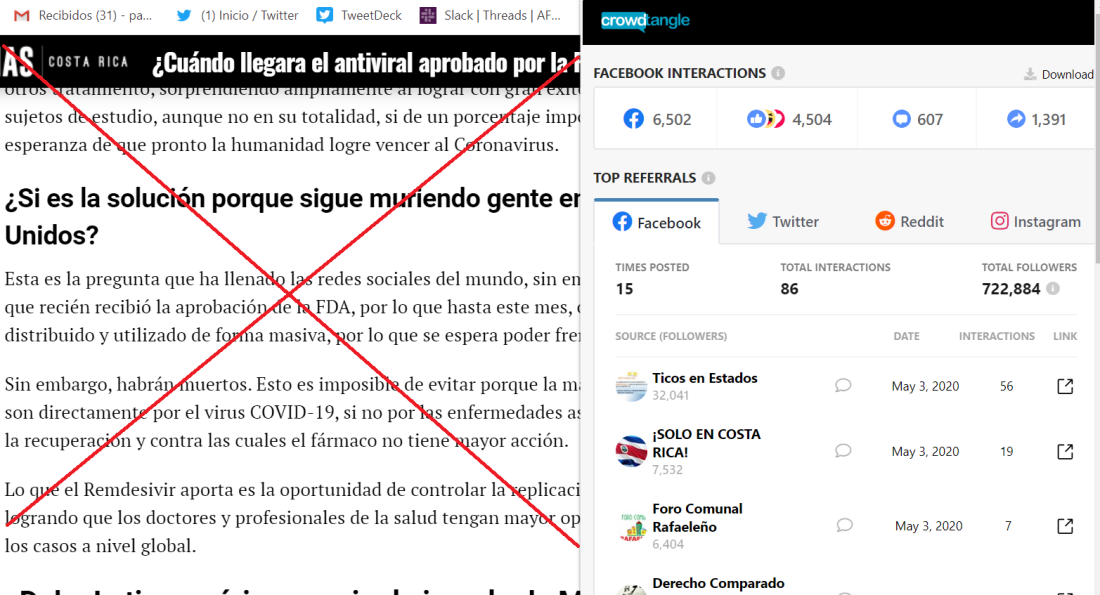
Captura de pantalla de un sitio web que publicó información sobre el remdesivir realizada el 22 de mayo de 2020
¿Qué es el remdesivir?
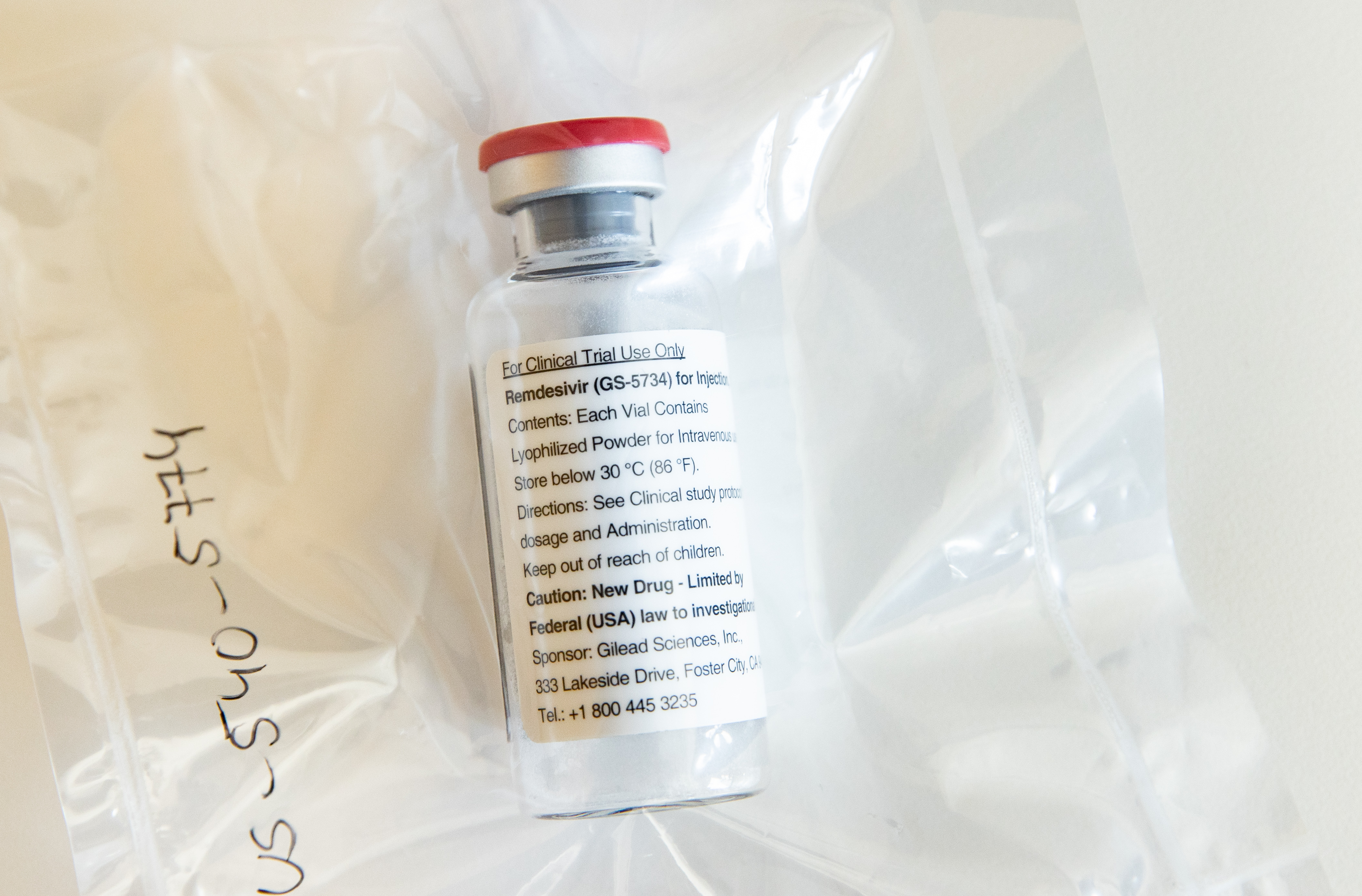
El remdesivir es un medicamento desarrollado por el laboratorio Gilead en Estados Unidos, que se usa en el tratamiento de pacientes con COVID-19, hospitalizados y en estado grave, desde que la autorización de uso urgente fue emitida por la FDA el 4 de mayo de 2020.
Según explica el laboratorio, el medicamento se administra por vía intravenosa. “La dosis óptima y la duración del tratamiento con remdesivir aún es desconocida”, dice, pero se sugiere administrarlo durante 10 días para pacientes que necesiten ventilación mecánica invasiva y/o una membrana oxigenante extracorporal.
Un tratamiento de cinco días se recomienda para pacientes que no requieran asistencia respiratoria, pero si no demuestra mejoría clínica durante esos días, el tratamiento puede extenderse hasta 10 días, indica.
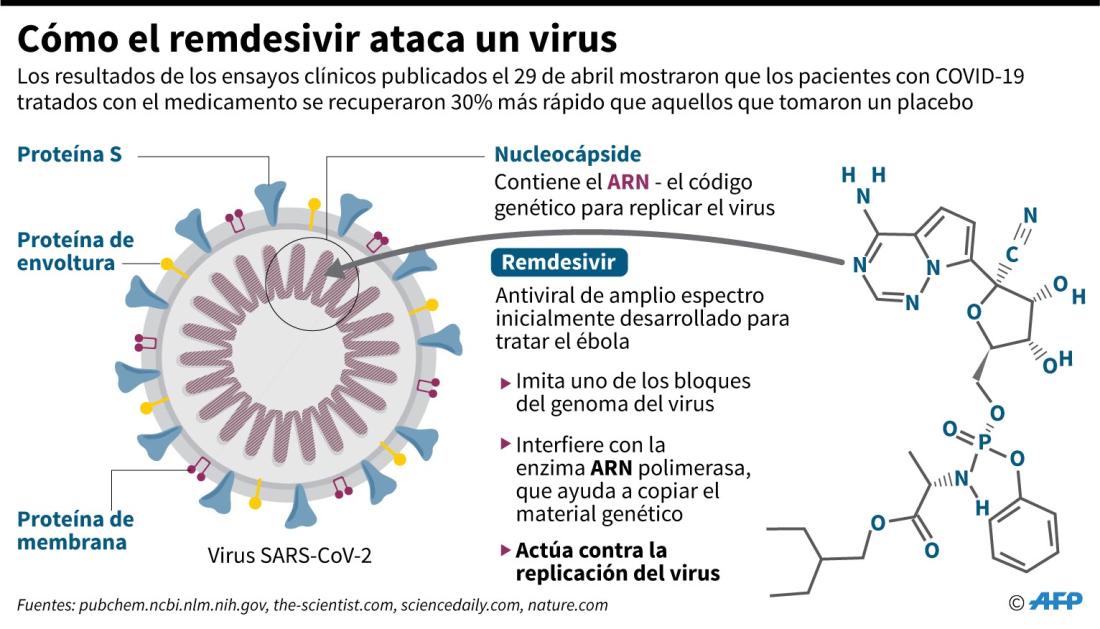
El remdesivir aprovecha una debilidad de los virus ARN (el código genético que permite que se repliquen), del que forman parte los coronavirus: durante la replicación pueden incorporar por error partes de esta molécula a su patrimonio genético, lo que los deja inoperativos.
En su página, Gilead aclara que el remedio “no ha sido aprobado en ningún lugar del mundo para ningún uso”. El laboratorio explica que el remdesivir tiene un “largo espectro en la actividad antiviral (...). Ha demostrado en actividad in vitro e in vivo en modelos animales su efecto contra los patógenos virales del MERS y SARS, los cuales son también coronavirus, con una estructura similar al COVID-19”.
“Los limitados datos preclínicos sobre el remdesivir en MERS y SARS indican que potencialmente podría tener actividad contra COVID-19”, añade.
Uso urgente
“A pesar de la escasa información sobre la seguridad y eficacia del uso de remdesivir para tratar a personas hospitalizadas con COVID-19”, la FDA emitió una autorización de uso urgente del medicamento el pasado 4 de mayo. Esto, debido a que “se demostró en un ensayo clínico que el medicamento en investigación reduce el periodo de recuperación en algunos pacientes”.
La autorización de uso urgente (EUA, por sus siglas en inglés), explica la FDA,“es diferente a la aprobación” que emite la propia agencia.
“Al determinar si se debe emitir una EUA, la FDA evalúa la evidencia disponible y compara cuidadosamente los riesgos conocidos o potenciales de los productos no probados con los beneficios conocidos o potenciales de ponerlo a disposición durante la emergencia”, indica la propia administración del gobierno estadounidense.
Según la FDA, la autorización de uso urgente es “la posibilidad de permitir el uso de productos médicos no aprobados durante una emergencia para realizar el diagnóstico, tratar o prevenir serias enfermedades que pueden ser amenazas para la vida (...) cuando no hay alternativas adecuadas, aprobadas y disponibles”.
José Peña, asesor regional de Asuntos Regulatorios, de la Organización Panamericana de la Salud, en la Unidad de Medicamentos Esenciales, Vacunas y Tecnologías de Salud, dijo a AFP Factual vía telefónica que el “remdesivir está siendo testeado en Estados Unidos, donde se aprobó de manera abreviada para hacer pruebas clínicas”.
Explicó que, aún con la autorización de uso urgente del remdesivir, no se han realizado los estudios a profundidad, aunque el fármaco ha demostrado que “tuvo claramente una mejor sobrevida” y un menor tiempo de hospitalización” entre los pacientes.
“Hoy en día nosotros no tenemos estudios clínicos robustos que nos permitan decir si para el tratamiento del COVID severo, crítico, este es el tratamiento a elegir”, dijo.
“Hay muchas experiencias con estudios de caso, que no es lo mismo que un estudio clínico controlado”, advirtió Peña, al explicar que se estudió a un grupo pequeño de pacientes, al que no se comparó con otro. Por lo tanto, señaló, no es suficiente la evidencia y no son estudios clínicos robustos.
Acceso en México
En la conferencia matutina que realizó el gobierno federal de México el 8 de mayo, el canciller Marcelo Ebrard declaró que se colabora con el laboratorio Gilead para que México tenga acceso en tiempo y forma al remdesivir, cuando el medicamento se ponga en circulación.
Ebrard añadió que, a raíz de una resolución de la Secretaría de Salud “se hizo un primer esfuerzo y una gestión exitosa para incluir a México [en los ensayos clínicos], que no estaba”. “Obviamente la instrucción fue que sí participáramos vía el Instituto Nacional de Nutrición”, señaló.
El 19 de mayo, durante la conferencia de prensa diaria sobre el coronavirus, el subsecretario de Prevención y Promoción a la Salud, Hugo López-Gatell, dijo que el uso del remdesivir “posiblemente es prometedor”, con resultados que entusiasman durante la actual pandemia, aunque modestos, y subrayó que faltaban varias fases de ensayos clínicos.
Pero aclaró: “No es un medicamento que esté autorizado para su uso generalizado, ni en México, ni en ninguna otra parte del mundo”.
Debate en torno al remdesivir
La comunidad científica debate sobre la efectividad del medicamento, debido a que los datos son contradictorios y parciales. La autorización de la FDA se basó en un gran ensayo público que concluyó que se reducía en cuatro días (en promedio) el restablecimiento de los pacientes, de 15 a 11 días.
Ese resultado es considerado "modesto" por numerosos investigadores, incluso si otros lo ven como una manera de reducir la saturación de los hospitales. Los resultados completos del estudio no fueron divulgados, suscitando críticas en la comunidad científica.
Además, el estudio no permite decir si el remdesivir reduce la mortalidad, porque la diferencia resultante (8% de los pacientes tratados, contra el 11,6% en el grupo testigo) está por debajo del umbral de fiabilidad estadística.
"Si hubiera 15% o incluso 10% de reducción de la mortalidad, no nos haríamos las mismas preguntas. Pero ahora hay un debate real" sobre si vale la pena ampliar el uso de esta molécula, dijo a la AFP el infectólogo franco-iraní Yazdan Yazdanpanah, quien dirige el consorcio de investigación REACTing, con sede en el Instituto Nacional de Salud e Investigación Médica de Francia.
Por lo tanto, aunque el medicamento remdesivir ha sido autorizado por la FDA para su uso en hospitales, fue una medida de urgencia, ya que aún no ha sido aprobado para uso masivo. Incluso, aún hay discusiones entre la comunidad científica sobre su efectividad e idoneidad en el tratamiento del COVID-19.
Copyright © AFP 2017-2025. Cualquier uso comercial de este contenido requiere una suscripción. Haga clic aquí para obtener más información.
¿Duda sobre la veracidad de una información, una foto o un video?
Contáctenos